
Chemisches Profil von Artemisia annua L.
Artemisia annua L. weist mit über 400 identifizierten Verbindungen ein außergewöhnlich komplexes Phytochemikalienprofil auf. Dieser Fachartikel klassifiziert die pharmakologisch relevanten Hauptstoffgruppen – Sesquiterpenlactone, Flavonoide, Terpenoide und Phenolsaeure – und dokumentiert Gehaltsvarianzen in Abhängigkeit von Genotyp, Herkunft, Erntezeitpunkt und Verarbeitungstemperatur. Analytische Standardmethoden und Qualitaetskriterien nach WHO-Monografie werden beschrieben.
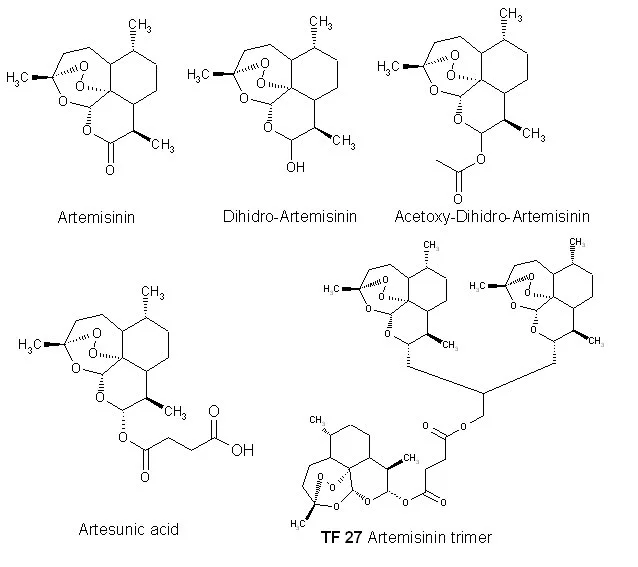
Artemisinin & Derivate: Struktur, Wirkmechanismus, Pharmakokinetik
Artemisinin (C15H22O5) vermittelt seine antiparasitäre Wirkung durch Häm vermittelte Spaltung der Endoperoxidbrücke mit konsekutiver Radikalbildung und Alkylierung parasitenspezifischer Proteine (u.a. PfATP6). Der Artikel beschreibt Pharmakokinetik, Autoinduktion über CYP2B6/3A4, Vergleich der semisynthetischen Derivate (Artesunat, Artemether, DHA) sowie den aktuellen Forschungsstand zur onkologischen Nutzung.
Synergieeffekte & Vielstoffgemisch: Pharmakologische Grundlagen
Casticin, Artemetin und Chrysosplenol-D aus Artemisia annua erhöhen die Artemisinin-Wirksamkeit durch Fe3+/Fe2+-Konversion und Hemmung des hepatischen First-Pass-Metabolismus. Ganzpflanzenextrakte zeigen bis zu 40-fach höhere Artemisinin-Plasmaspiegel gegenüber Reinsubstanz (WPI 2012/2022). Zusätzlich verlangsamen Vielstoffgemische die Entwicklung von Plasmodium-Resistenzen signifikant (PNAS 2015).

Biosynthese & Regulation der Artemisinin-Produktion
Die Artemisinin-Biosynthese läuft ausschließlich in glandulären Drüsentrichomen ab und folgt dem Präsidieren MEP-Pfad. Die Enzymmkaskade (ADS → CYP71AV1/CPR → ALDH1) wird durch einen nicht-enzymatischen photo-oxidativen Abschlussschritt komplettiert. Regulatorische Einflussgrößen umfassen AaFT2 (Blütregulatoin), UV-B-Exposition (+9–11 % Trichomzahl), abiotischen Stress und Erntezeitpunkt.

Toxikologie & Sicherheitsprofil: Präklinische und klinische Daten
Artemisia annua weist eine orale LD50 von 4.228–5.105 mg/kg (Maus, Artemisinin rein) bzw. >5.000 mg/kg (wässriger Extrakt) auf. Klinisch relevante Sicherheitsaspekte umfassen Embryotoxizität im ersten Trimester, CYP2B6/CYP3A4-vermittelte Arzneimittelinteraktionen (Antikoagulanzien, Immunsuppressiva), QTc-Verlängerung bei Artemether/Lumefantrin sowie seltene Ototoxizität bei hochdosiertem Artesunat.
